国务院于2026年1月27日正式公布了新修订的《中华人民共和国药品管理法实施条例》(以下简称“《条例》”),《条例》自2026年5月15日起施行。这是该《条例》自2002年施行以来的首次全面修订,修订条款达到90%以上,除了第一条以《药品管理法》(“《药管法》”)作为立法依据的条款未被修改外,其余条款均有调整或者修订。《条例》将原有的“以对药品生产经营企业的管理为中心”的监管逻辑,全面转变为“以药品上市许可持有人(下称“MAH”)为中心”,实现药品全生命周期监管逻辑的系统性重塑。
本文通过对《条例》新旧条款的深度对比分析,拆解修订的核心要点与监管导向,为医药行业企业提供专业、贴合实操的法规解读。《条例》共设总则、药品研制和注册、药品上市许可持有人、药品生产、药品经营、医疗机构药事管理、监督管理、法律责任、附则九个章节,共计八十九条规定,不仅全面细化《药管法》的制度措施和监管要求,并且聚焦药品全生命周期监管,突出鼓励创新、知识产权保护、安全监管等方面,注重规则细化与实操性衔接,为药品研制、生产、经营、使用和监督管理活动提供了系统、明确的法规指导。
一、修订核心背景
现行《条例》(2024年版)自2002年施行以来,虽历经2016年、2019年、2024年三次局部修改,但其框架和内容已难以适配2015年药品审评审批制度改革、2019年《药管法》全面修订后的新监管体系和实践要求。2022年虽《中华人民共和国药品管理法实施条例(修订草案征求意见稿)》曾向社会公开征求意见,但其中多数内容后续未被正式采纳实施。
此次修订将2015年以来药品监管改革中成熟的经验(如药品上市许可持有人制度、优先审评、附条件批准等)正式上升为行政法规,填补药品研制、生产、流通、使用各环节的法规监管盲区。《条例》立足于人民群众的用药需求,关注儿童患者、罕见病患者、老年患者用药权益的保障,完善药品全生命周期监管规则,推动药品高水平安全与医药产业高质量发展良性互动。
二、核心条款新旧对比(四大关键领域)
本次修订围绕药品全生命周期监管逻辑,从药品研制与注册、药品生产管理、药品经营与使用、药品安全监管四大核心领域展开条款优化与制度完善,以下结合新旧条例内容展开深度对比,解读修订亮点并提供企业合规建议。
(一)药品研制与注册:强化创新支持,完善知识产权保护制度
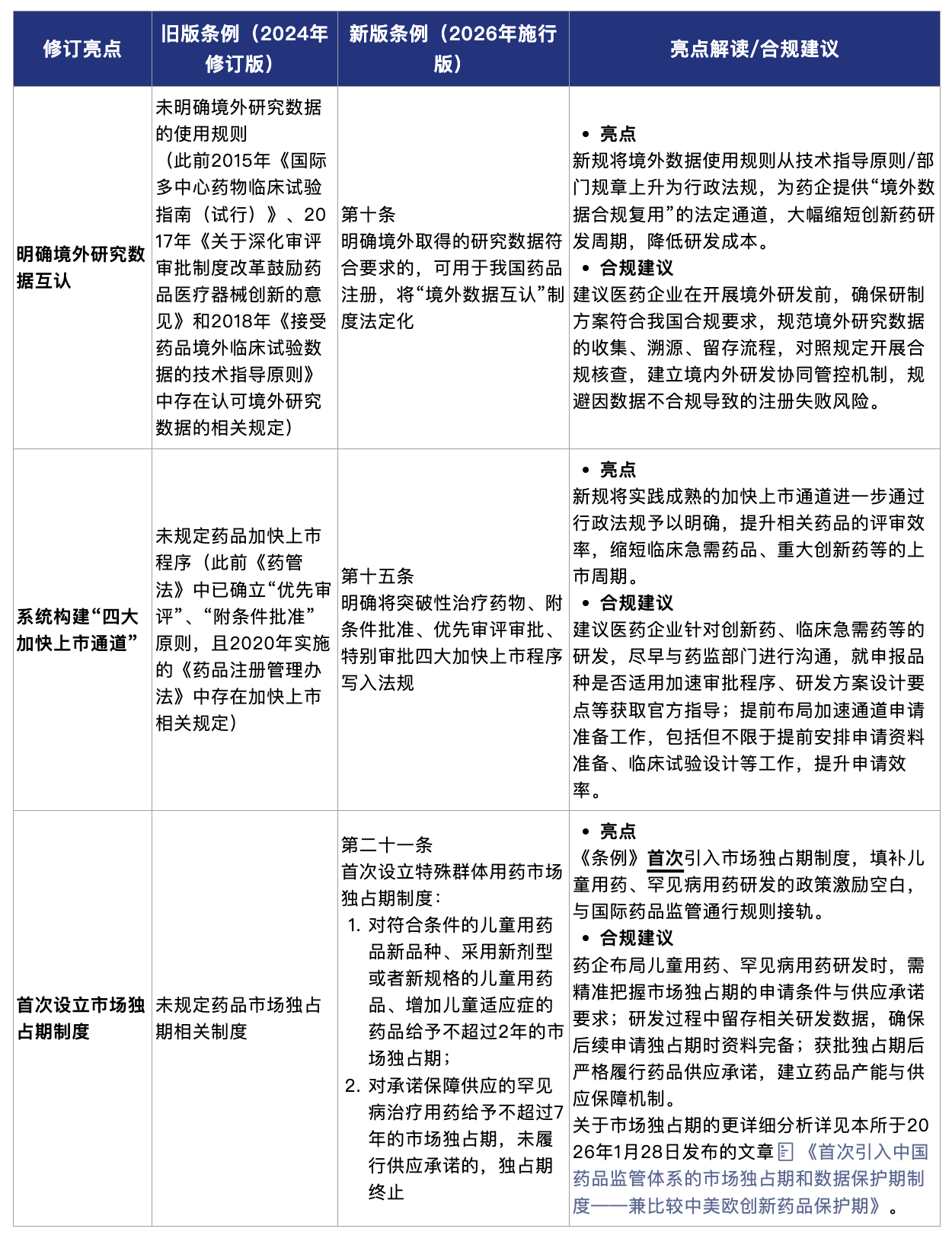
(二)药品生产管理:优化生产模式,强化中药全链条监管
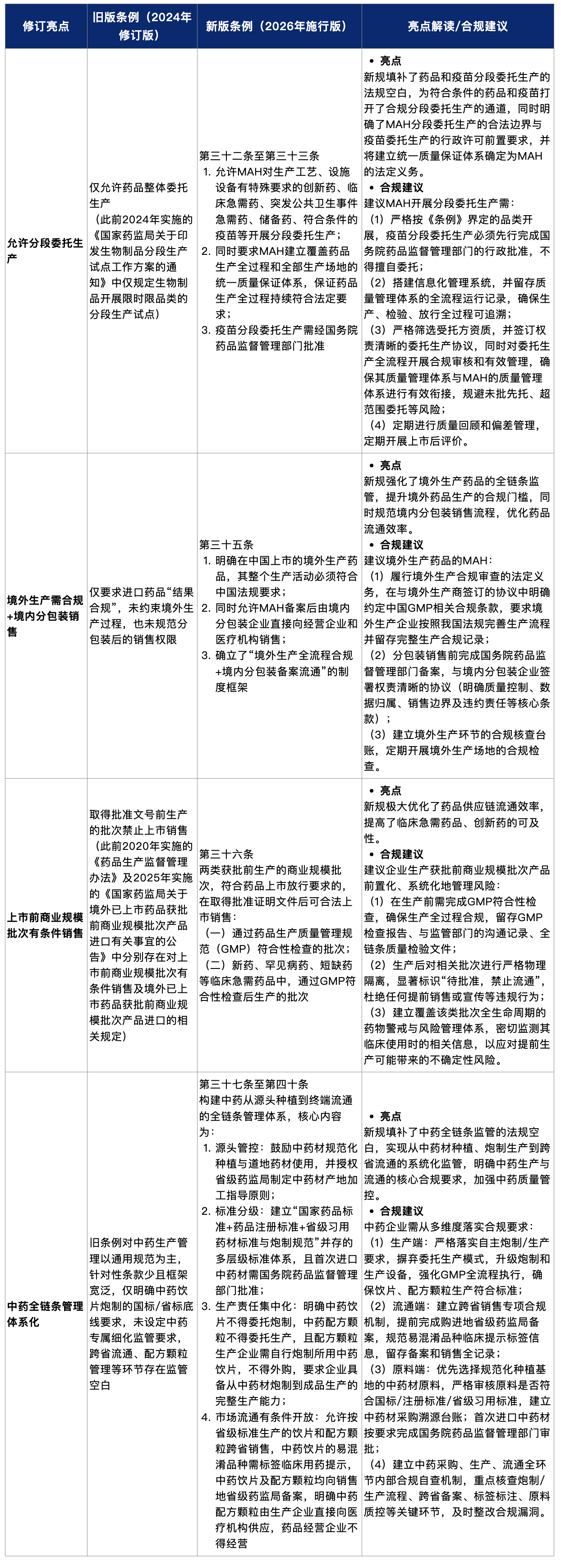
(三)药品经营与使用:规范网络售药,优化医疗机构制剂监管

(四)药品安全监管:细化监管措施,加大全链条处罚力度

三、结语
此次《条例》的全面修订,既是对2019年修订的《药管法》相关制度要求的细化落地与实操化衔接,也是对我国2015年以来药品监管改革成果的固化升级,进一步通过行政法规予以确认。本次修订围绕“人民至上、生命至上”的理念,以药品上市许可持有人为监管核心,构建起全生命周期、全链条的药品监管体系。
对于医药企业而言,本次《条例》修订带来了全新的监管要求与发展机遇,企业需精准把握政策调整方向,全面梳理企业内部研发、生产、经营、使用各环节的合规体系,提前布局企业内部合规体系的优化调整,在享受创新红利的同时,守住质量安全底线。
距离《条例》正式施行尚有不足三个月时间,建议医药企业尽快将合规调整工作纳入企业重点工作,确保在新规施行前实现全环节的合规落地。环球律师事务所生命科学及医疗团队将持续跟踪配套政策的出台与实施情况,为医药企业提供专业的法规解读与合规指导。